NộI Dung
Các phần khácNguyên tử là cơ sở xây dựng của mọi vật chất. Các loại nguyên tử khác nhau được gọi là "nguyên tố" và chúng được tổng hợp thành một biểu đồ gọi là bảng tuần hoàn. Bảng cho phép các nguyên tố tương tự được nhóm lại với nhau dựa trên tính chất hóa học của chúng. Điều thú vị là các nguyên tử trong cùng một nhóm cũng thường có các tính chất vật lý tương tự nhau. Nếu bạn muốn hiểu được các tính chất hóa học và vật lý của nguyên tử, hãy học cách chia bảng tuần hoàn thành các nhóm và nghiên cứu từng tính chất của mỗi nhóm.
Các bước
Phương pháp 1/3: Phân chia bảng tuần hoàn
Xác định vị trí của các nguyên tố là phi kim. Trong bảng tuần hoàn, phần lớn các nguyên tử được xếp vào nhóm kim loại. Các nguyên tử khác được xếp vào nhóm phi kim. Bạn sẽ thấy những nhóm này có lợi khi bạn khám phá các thuộc tính của các nguyên tử khác nhau.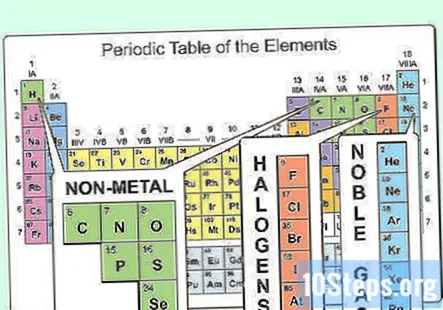
- Các phi kim có thể được tìm thấy chủ yếu ở góc trên bên phải của bảng tuần hoàn, trong khi phần còn lại của bảng chủ yếu bao gồm kim loại. Hydro là một ngoại lệ đối với quy tắc này, vì nó hoạt động giống như một phi kim trong điều kiện tiêu chuẩn, nhưng nó được tìm thấy ở góc trên bên trái của bảng.
- Cacbon, nitơ, oxy, hydro, lưu huỳnh và khí quý (các nguyên tố ở cột ngoài cùng bên phải) là những phi kim thường được biết đến.
- Các halogen (như flo, clo, brôm, v.v.) thuộc loại phi kim.

Phân biệt các nhóm kim loại chính. Kim loại được nhóm thành các danh mục phụ. Các nguyên tố trong các danh mục con này giống nhau theo những cách cụ thể hơn là chỉ xác định cả hai là kim loại. Các loại phổ biến là kim loại kiềm, kim loại kiềm thổ, kim loại chuyển tiếp, kim loại sau chuyển tiếp, lantan và actinide.- Các kim loại kiềm rất dễ phản ứng và dễ bị ion hóa ở trạng thái 1.
- Các kim loại kiềm thổ phản ứng kém hơn một chút, nhưng dễ dàng ion hóa ở trạng thái 2.
- Kim loại chuyển tiếp và sau chuyển tiếp bền hơn và có nhiều trạng thái ion hóa khác nhau.
- Lanthanides và actinides là những phân tử lớn hơn, kém ổn định hơn, dễ dàng phản ứng. Một số trong số chúng bị phân hủy, khiến chúng có tính phóng xạ.

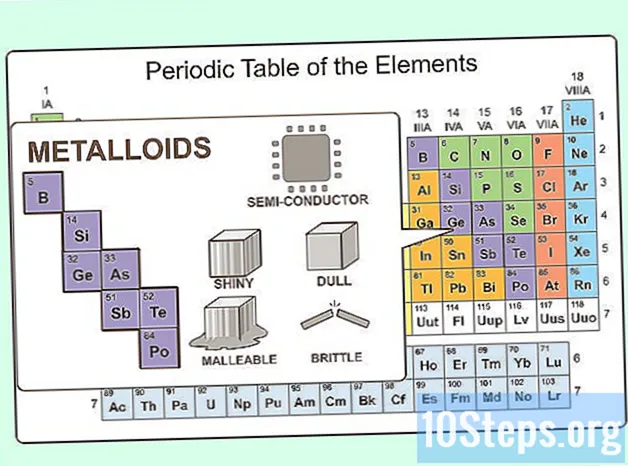
Hãy tưởng tượng một cái gì đó giữa kim loại và phi kim. Các nguyên tố như vậy thực sự tồn tại và chúng được gọi là kim loại. Trong bảng tuần hoàn, các kim loại xuất hiện giữa kim loại chuyển tiếp và phi kim. Có tám kim loại:- Boron
- Silicon
- Gecmani
- Thạch tín
- Antimon
- Tellurium
- Polonium
- Astatine
Phương pháp 2/3: Phân tích đặc điểm hóa học

Nhìn vào thứ tự của bảng. Khi bạn nhìn vào bảng tuần hoàn, bạn sẽ nhận thấy rằng các nguyên tố đều được đánh số. Đánh số này không phải là ngẫu nhiên. Trên thực tế, nó được gọi là số nguyên tử của nguyên tố cụ thể đó và bằng số proton mà nguyên tố có trong hạt nhân của nó.- Đối với nguyên tử (không phải ion), số hiệu nguyên tử cũng biểu thị số electron trong nguyên tử. Số proton và electron trong nguyên tử bằng nhau.
- Trên một số bảng tuần hoàn, bạn sẽ nhận thấy số thứ hai có phông chữ nhỏ hơn. Đây là khối lượng nguyên tử trung bình của nguyên tố đó.
Hình dung các electron hóa trị. Các điện tử hóa trị là các điện tử ở lớp vỏ ngoài cùng của đám mây điện tử nguyên tử. Các electron hóa trị là yếu tố lớn nhất trong cách nguyên tử sẽ phản ứng hóa học. Cấu hình ổn định nhất của một nguyên tử là có các electron ở lớp vỏ ngoài cùng được lấp đầy, do đó nó sẽ không liên kết với các nguyên tử khác. Trong hầu hết các trường hợp, lớp vỏ ngoài cùng cần chứa đủ 8 electron (tùy thuộc vào kích thước của nguyên tử mà lớp vỏ này có thể khác nhau).
- Ví dụ, flo có chín electron. Hai cái đầu tiên điền vào orbital trong cùng, bảy cái còn lại là các electron hóa trị. Điều này có nghĩa là flo chỉ cần thêm một điện tử nữa để lấp đầy lớp vỏ hóa trị của nó. Do đó, flo dễ dàng phản ứng với các nguyên tử có thể nhường electron (đặc biệt là kim loại).
- Một ví dụ về điều ngược lại là liti. Liti có ba electron. Hai cái đầu tiên lấp đầy lớp vỏ trong cùng và cái cuối cùng là một electron hóa trị. Vì liti cần phải thu được bảy điện tử để lấp đầy lớp vỏ hóa trị của nó, nên việc loại bỏ một điện tử hóa trị duy nhất mà nó có sẽ dễ dàng hơn (thuận lợi hơn về mặt năng lượng). Vì vậy, liti dễ dàng phản ứng với các nguyên tố chấp nhận một điện tử (như halogen).
Xem xét kích thước của nguyên tử. Mặc dù các điện tử hóa trị là yếu tố dự đoán tốt nhất về các tính chất hóa học trong một nguyên tử nhất định, nhưng kích thước của nguyên tử cũng rất quan trọng. Các nguyên tử lớn hơn có nhiều electron hơn giữa hạt nhân và các electron hóa trị, có nghĩa là chúng được giữ chặt vào nguyên tử lỏng lẻo hơn so với các nguyên tử nhỏ hơn. Điều này giải thích tại sao hai nguyên tử có cùng số electron hóa trị (ví dụ, flo và clo) có các tính chất hóa học tương tự, nhưng không giống nhau.
Tìm hiểu xu hướng của bảng tuần hoàn. Biết xu hướng tuần hoàn có thể giúp bạn nhận ra các tính chất hóa học có thể có của một nguyên tố dựa trên vị trí của nó trong bảng tuần hoàn. Tuy nhiên, điều quan trọng cần nhớ là ba nhóm (khí quý, lantan và actinide) không tuân theo các xu hướng này do đặc tính hóa học độc đáo của chúng. Một số xu hướng định kỳ là:
- Khối lượng nguyên tử tăng dần từ trái sang phải và từ trên xuống dưới.
- Bán kính nguyên tử giảm dần từ trái sang phải và tăng từ trên xuống dưới.
- Độ âm điện tăng từ trái sang phải và giảm từ trên xuống dưới.
- Năng lượng ion hóa tăng từ trái sang phải và giảm từ trên xuống dưới.
- Ái lực của electron tăng từ trái sang phải và giảm từ trên xuống dưới.
- Ký tự kim loại giảm từ trái sang phải và tăng từ trên xuống dưới.
Phương pháp 3/3: Kiểm tra các thuộc tính vật lý
Nhận biết tính chất của phi kim. Phi kim tồn tại ở ba trạng thái vật lý ở nhiệt độ phòng (rắn, lỏng và khí), nhưng chủ yếu là chất khí ở nhiệt độ phòng. Phi kim thường xỉn và giòn khi ở thể rắn, và chúng thường nóng chảy và sôi ở nhiệt độ thấp hơn kim loại. Phi kim cũng là chất dẫn nhiệt và dẫn điện kém.
- Phi kim duy nhất là chất lỏng ở nhiệt độ thường là brom.
- Cacbon có nhiệt độ nóng chảy cao nhất trong tất cả các nguyên tố.
Biết tính chất vật lý của kim loại. Kim loại sáng bóng và dễ uốn. Chúng cũng dẫn nhiệt và dẫn điện tốt. Các kim loại chủ yếu là rắn ở nhiệt độ phòng, mặc dù thủy ngân là chất lỏng. Các kim loại thường có nhiệt độ nóng chảy và nhiệt độ sôi cao so với phi kim.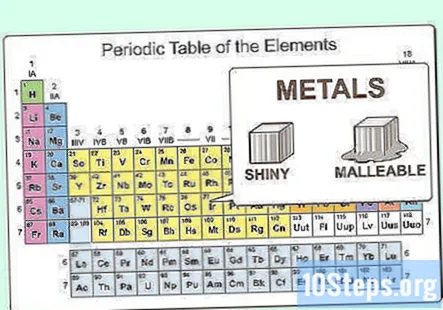
Lưu ý các khí quý. Các nguyên tố tạo nên cột ngoài cùng bên phải được gọi là khí quý. Chúng trơ về mặt hóa học và đều được tìm thấy trong pha khí ở nhiệt độ phòng. Những loại khí này được sử dụng cho những thứ như làm đầy bóng bay và chiếu sáng các biển báo.
Hãy xem xét các kim loại. Giống như các kim loại có tính chất hóa học của cả kim loại và phi kim, chúng có tính chất vật lý của cả hai. Chúng là chất bán dẫn. Chúng có thể dễ uốn hoặc giòn. Chúng cũng có thể sáng bóng hoặc xỉn màu.
Câu hỏi và câu trả lời của cộng đồng
Có phải độ âm điện đang tăng lên trong một nhóm không?

Nhà nghiên cứu Khoa học Meredith Juncker là ứng viên Tiến sĩ về Hóa sinh và Sinh học Phân tử tại Trung tâm Khoa học Sức khỏe Đại học Bang Louisiana. Các nghiên cứu của cô tập trung vào protein và các bệnh thoái hóa thần kinh.

Lời khuyên
- Bạn có thể tạo thẻ ghi chú để nghiên cứu các nhóm yếu tố khác nhau.
- Nếu bạn được phép sử dụng bảng tuần hoàn trong các bài kiểm tra và bài kiểm tra, bạn có thể sử dụng bảng tuần hoàn để tìm ra nhiều câu trả lời.
Cảnh báo
- Có rất nhiều thông tin chứa trong bảng tuần hoàn. Hãy dành thời gian của bạn và học hàng ngày thay vì cố gắng duy trì nó trong một buổi học nhồi nhét.